Número 022 2006 Revista Internacional de Psicoanálisis en Internet
Cannabis: informe de la Comisión Clínica de la Delegación del Gobierno para el Plan Nacional sobre Drogas
Autor: Comisión Clínica de la Delegación del Gobierno para el Plan Nacional sobre DrogasPalabras clave
Cannabis, Hachis, Marihuana, Tetrahidrocannabinol (thc).
En Aperturas Psicoanalíticas pensamos que sería de enorme utilidad para los lectores el disponer de la información que la Comisión Nacional sobre Drogas del Ministerio de Sanidad de España acaba de hacer pública en Marzo del 2006 acerca del uso del cannabis, puesto que recopila la información actualizada sobre el tema en base a datos contrastados. A continuación incluiremos, de manera textual, aquellos sectores del informe que consideramos conveniente destacar.
4. Edad de inicio en el consumo de cannabis, y efectos adversos
La edad de inicio en el consumo del cannabis parece ser un factor determinante en la aparición y gravedad de las consecuencias negativas de su consumo. Así, los problemas y trastornos parecen ser más pronunciados entre aquellos que inician el consumo antes de los 16 años, probablemente con relación a que el cannabis provoca cambios neurobiológicos durante determinados periodos del desarrollo del cerebro [Ehrenreich et al., 1999; Pistis et al., 2004].
Los resultados de los distintos estudios permiten afirmar que el inicio temprano en el consumo de cannabis se asocia por un lado, con aparición de trastornos mentales [Arsenault et al., 2002; Fergusson et al 2002;
Lynskey et al., 2004; Stefanis et al., 2004]; por otro lado, con un consumo importante y problemático de cannabis u otras drogas en edades posteriores [Grant & Dawson 1998; Lynskey et al., 2003]; y con mayor dificultad para abandonar el consumo [DeWit et al., 1997]. Finalmente la edad de inicio temprana del consumo de cannabis se ha observado que también se asocia con mayores problemas de déficit neuropsicológicos y por tanto más problemas de rendimiento secundarios, que en los adolescentes puede traducirse en un peor rendimiento escolar y en el abandono prematuro de los estudios. [Fergusson et al., 1997; Hall et al. 2001; Pope et al., 2003; Fergusson et al. 2002].
Así pues, la fase inicial de la adolescencia parece ser un periodo de crucial importancia para el desarrollo del daño relacionado con cannabis.
Aunque la asociación entre consumo temprano de cannabis y problemas posteriores puede ser debida en parte a factores de riesgo comunes (genéticos, de personalidad, sociológicos), es importante, desde la perspectiva de salud publica, monitorizar la edad de inicio del primer consumo, puesto que un descenso en la edad del consumo es probable que resulte en una mayor exposición acumulada a lo largo de la vida y aparición de más problemas y trastornos.
5. Efectos agudos del cannabis
La Cannabis sativa es una planta que contiene más de 400 componentes químicos, de las cuales se conocen al menos 60 cannabinoides que son únicos de la especie. Los tres cannabinoides más importantes, por sus efectos psicoactivos, son el delta-9-tetrahidrocannabinol (THC), el cannabidiol y el cannabinol.
El contenido de cannabinoides depende de varios factores como la parte de la planta, el tipo (existen distintos genotipos o variedades) y el momento en que es recolectada. La mayor concentración de cannabinoides se encuentra en los brotes florecientes de la planta femenina y en las hojas, mientras que las concentraciones son bajas en el tallo, raíces y semillas.
El cannabis se presenta para su consumo en forma de hachís, que es un exudado resinoso de la planta, como un triturado seco de flores, hojas y pequeños tallos de la propia planta triturada (marihuana, maría) y como aceite. Se consume habitualmente fumada, mezclada con tabaco o directamente mediante vaporizadores. También puede utilizarse el aceite por vía oral.
Habitualmente la marihuana contiene entre un 1-5% de THC, el hachís entre un 15-50% y el aceite entre un 25-50%. El cannabis utilizado para producir fibra textil tiene una riqueza de THC inferior al 0.3%. Asumiendo que un cigarrillo de marihuana pesa 0,8 g. el contenido de THC estaría comprendido entre 8 y 120 mg. [Ashton, 2001].
Parece ser que la potencia del cannabis ha ido aumentando progresivamente en los últimos años. Habrían contribuido las técnicas de autocultivo y la selección genética de las variantes más psicoactivas, que han hecho que se puedan encontrar variedades con hasta un 20% de THC. Aún así, la potencia media del cannabis en Europa en los últimos años se ha mantenido estable [EMCDDA, 2004].
El THC y los demás cannabinoides se unen a unos receptores llamados cannabinoides (CB1 y CB2). Estos receptores se encuentran en la membrana de algunas células y están acoplados a la proteína G como sistema de transducción. El receptor CB1 está presente fundamentalmente en el sistema nervioso central y en menor densidad en sistema nervioso periférico mientras que el receptor CB2, de localización fundamentalmente periférica, se encuentra principalmente en células del sistema inmunológico. Los receptores cannabinoides están ampliamente distribuidos en el cerebro.
Existen compuestos endógenos que se unen a estos receptores y a los que se denomina como endocannabinoides. Estos ligandos pueden también modular la transmisión sináptica de los neurotransmisores glutamato y ácido gamma-aminobutírico (GABA) así como actuar sobre la neurotransmisión postsináptica dopaminérgica. Aunque no está del todo aclarado, el sistema endocannabinoide podría estar implicado en diferentes funciones fisiológicas entre las que destacan el aprendizaje, la memoria, las emociones, el refuerzo, la ingesta de comida, la neuroprotección, el dolor y la conducta motora, entre otras [Pertwee, 2004; Howlett et al., 2004]. El THC como otras drogas de abuso actúa sobre el sistema cerebral de recompensa (mesocorticolímbico) que incluye el área ventral tegmental, el núcleo accumbens y la corteza prefrontal entre otras áreas cerebrales. El THC aumenta la liberación de dopamina en el núcleo accumbens (Figura 9).
.jpg)
FIGURA 9. Sistema cerebral de recompensa donde actúa el THC y las otras drogas de abuso produciendo liberación de dopamina en el núcleo accumbens. Se muestran en punteado rojo las áreas cerebrales donde se encuentran los receptores cannabinoides (modificada de NIDA)
El cannabis habitualmente se fuma (vía intrapulmonar), ya que ésta es la vía de consumo más eficiente. Del total de THC contenido en un cigarrillo, entre un 10-30% llega a los pulmones y la sangre, un 30% se destruye por la combustión y un 50% se pierde en el aire. La cantidad final de THC absorbido en el organismo depende de la profundidad y número de caladas y de la potencia de los cigarrillos. El THC se detecta en sangre inmediatamente después de la primera calada (1-2 minutos) y las concentraciones máximas se alcanzan entre los 3 y 10 minutos.
Los efectos se inician entre segundos y minutos tras haber consumido la sustancia y persisten hasta 2 y 3 horas. Cuando el cannabis se administra por vía oral (aceites, pasteles, infusiones) la absorción es lenta y errática, la concentración máxima de THC en plasma aparece a las 2-4 horas y el inicio de los efectos se da entre media hora y 2 horas postadministración, pudiendo durar los mismos unas 6 horas. La presencia de comida puede retrasar la absorción de THC [Grotenhermen, 2003; Huestis, 2005].
El THC es una molécula muy lipofílica por lo que atraviesa con facilidad la barrera hematoencefálica (BHE) y la placentaria. El THC se acumula en la leche materna (8 veces más que en el plasma). Por esta afinidad a los lípidos se une a la grasa corporal, lo que provoca una prolongación de sus efectos y de su acumulación en el organismo. El THC se convierte rápidamente en el hígado en 11-hidroxi-THC (11-OH-THC) que es activo y después a 11-nor-9-carboxi-THC (THCCOOH) que es un metabolito inactivo. Se han identificado alrededor de 100 metabolitos del THC. La semivida de eliminación del THC, es decir el tiempo que tarda en reducirse a la mitad la concentración en la sangre, es de 25-36 horas. Un 80% se elimina a través de las heces y un 20% en la orina como THC-COOH y otros metabolitos. Las pruebas para determinar el consumo de THC se basan en la detección de su metabolito (THC-COOH). Tras el consumo de un cigarrillo puede detectarse el metabolito de THC en orina (orina positiva) durante una semana. En consumidores crónicos la orina puede ser positiva hasta más de un mes después de dejar de consumir [Grotenhermen 2003; Huestis 2005].
En los apartados siguientes de este epígrafe se describen los principales efectos farmacológicos producidos por el cannabis.
5.1. Efectos sobre el Sistema Nervioso Central (SNC)
Los efectos sobre el SNC son los más relevantes ya que constituyen la base de su abuso y se asocian a algunas de las complicaciones más frecuentes tras el consumo agudo y crónico (Tabla 4).
Tabla 4. Efectos centrales agudos del cannabis

5.1.1. Efectos psicológicos agudos
Los preparados del cannabis, hachís y marihuana principalmente, se han utilizado desde hace muchos años por sus propiedades psicoactivas. El principal responsable de la actividad farmacológica psicoactiva es el delta-9-tetrahidrocannabinol (THC) y su administración aislada produce efectos similares al cannabis en humanos [Wachtel y col, 2002]. Los efectos de los otros cannabinoides y otros compuestos contenidos en la planta pueden producir acciones aditivas o antagonistas de las del THC. Así por ejemplo el cannabidiol (CBD) provoca efectos sedantes y ansiolíticos.
Los efectos agudos del cannabis son muy variables entre personas y dependen de la dosis, del contenido de THC, de la proporción THC/CBD, de la forma de administración, así como de la personalidad, las expectativas y experiencia previa del sujeto y también del contexto en que se consume [Camí y Cols, 1989].
El consumo de cannabis produce generalmente un efecto bifásico. Tras una fase inicial de estimulación (euforia, bienestar, aumento de la percepción, ansiedad), le sigue una fase donde predomina la sedación (relajación, somnolencia, sueño). Se produce una agudización de las percepciones visuales, auditivas y táctiles, así como una ligera distorsión del espacio y tiempo. También aparece risa fácil, locuacidad y aumento del apetito. Paralelamente se altera la memoria reciente, y existe dificultad en la concentración, disminución de la atención e incoordinación motora [Asthon, 2001; Abanades et al., 2005].
Aunque es difícil calcular las dosis habitualmente consumidas así como su biodisponibilidad, se sabe que una dosis fumada de 5 mg de THC proporciona unos efectos leves, que serían similares a los de 10 mg por vía oral. Dosis mayores pueden producir efectos intensos.
En algunos sujetos, especialmente en inexpertos o tras dosis elevadas puede aparecer ansiedad, disforia, síntomas paranoides y/o pánico, que habitualmente desaparecen de forma espontánea en pocas horas. Como se comenta más adelante, la intoxicación aguda por cannabis puede cursar con un episodio psicótico agudo que se caracteriza por ideas delirantes, alucinaciones, confusión, amnesia, ansiedad y agitación. Habitualmente estos cuadros agudos desaparecen espontáneamente a las pocas horas a medida que el THC se elimina del organismo.
5.1.2. Efectos cognitivos, sobre el rendimiento psicomotor y la conducción de vehículos.
El consumo agudo de cannabis altera la capacidad cognitiva (atención, memoria, percepción, resolución de problemas) y el rendimiento psicomotor. Los efectos son similares a los producidos por el alcohol y las benzodiazepinas e incluyen enlentecimiento en la velocidad de reacción, incoordinación motora, alteración de la memoria a corto plazo, dificultades de concentración y afectación de la atención dividida. Estos efectos son dosis-dependiente y alteran la habilidad en el momento de conducir un vehículo o manejar maquinaria de precisión.
En un metaanálisis de 87 estudios sobre el efecto del cannabis sobre distintas pruebas de rendimiento psicomotor, se demostró que el deterioro provocado por el cannabis en estas pruebas era máximo 1 hora después de ser fumado y entre 1 y 2 horas después de ser ingerido por vía oral. Pudo además establecerse una relación dosis-efecto. Cuando la dosis de cannabis está entre 200 y 300 microgramos/kilo de peso, equivalentes a un cigarrillo conteniendo entre 14 y 21 mg de THC en una persona de 70 kg, los efectos deletéreos son similares a los inducidos por el alcohol a concentraciones en sangre ≥0.5 gr/l [Ramaekers y cols., 2004]. La afectación psicomotora se incrementa al combinar el cannabis con etanol u otros sedantes.
Los efectos citados anteriormente se han demostrado en condiciones de laboratorio y en estudios experimentales de conducción de vehículos en circuitos cerrados o con tráfico. Los efectos del cannabis en cuanto a la seguridad vial y su implicación en los accidentes de circulación se han estudiado en muestras de accidentados en los que se ha demostrado la presencia de cannabinoides en la sangre u orina. Estos estudios observacionales comparten las limitaciones metodológicas comunes a todos los estudios naturalísticos: la existencia de otros factores que podrían ser relevantes (estado previo del sujeto) así como la imposibilidad de poder controlar de forma clara la cantidad de cannabis consumida. También hay que destacar que como el consumo de cannabis suele realizarse de forma conjunta con otras sustancias (alcohol principalmente), este patrón de policonsumo dificulta que pueda establecerse una asociación causal clara entre el consumo del cannabis y los accidentes.
Existen estudios que demuestran un mayor riesgo de colisiones, con resultado de lesiones y muerte en las personas que conducen bajo los efectos de cannabis. Los resultados de un estudio australiano muestran que el consumo de cannabis en las 3 horas previas a la colisión de tráfico se asoció a un riesgo casi cuatro veces mayor de ingreso hospitalario/ muerte en dicha colisión [Blows et al., 2005]. En un reciente estudio francés, que incluyó 10.748 conductores implicados en colisiones de tráfico mortales y de los que se disponía de información analítica sobre la presencia de alcohol y drogas, se observó que la presencia de cannabis se asociaba a un riesgo tres veces mayor de colisión [Laumon et al., 2005].
5.1.3. Efectos sobre el sueño
El THC induce sueño, probablemente debido al aumento de melatonina y altera el patrón sueño-vigilia. Tras la administración continua de dosis elevadas se puede observar durante la mañana siguiente un cierto grado de resaca en algunos sujetos. Además puede aparecer un efecto rebote en la cantidad de sueño REM tras la interrupción brusca de consumos elevados.
5.1.4. Efectos sobre la conducta alimentaria
El cannabis produce un aumento del apetito entre 1-3 horas tras su consumo. Tanto el THC por vía oral como el cannabis fumado aumentan el número de ingestiones y la cantidad total de comida ingerida. Sin embargo, con el consumo continuado de cannabis se produce una cierta disminución de este efecto.
5.1.5. Otros efectos
Los cannabinoides han demostrado ser analgésicos en modelos animales de dolor agudo y crónico. En humanos estas propiedades no se han demostrado claramente en el dolor agudo. En dolor crónico se ha aprobado en Canadá un preparado para el tratamiento del dolor neuropático en la esclerosis múltiple (ver usos terapéuticos).
Efectos sistémicos
El consumo de cannabis produce una alteración de la mayoría de sistemas del organismo. A continuación se describen los más relevantes (Tabla 5).
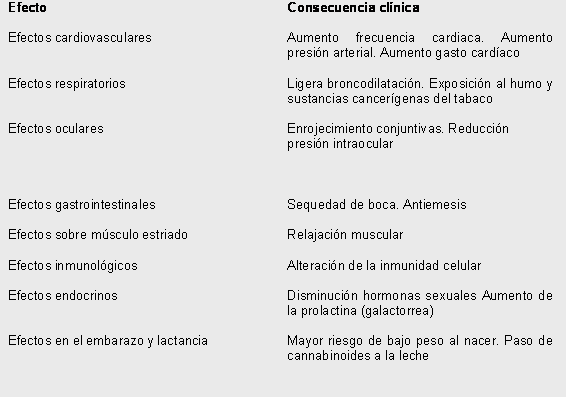
Tabla 5. Efectos sistémicos agudos del cannabis
5.2.1. Efectos cardiovasculares
Consisten básicamente en un aumento de la frecuencia cardiaca (20- 50%). Los efectos sobre la presión arterial comprenden un incremento de la misma si se está sentado o acostado y una disminución de la misma si se está de pie. Si la persona que fuma se levanta rápidamente puede aparecer sensación de mareo, hipotensión (ortostática) e incluso pérdida de conocimiento. Esto es más frecuente en sujetos con poca experiencia. Estos efectos dependen de la dosis y son máximos pocos minutos después de iniciar el consumo fumado y desaparecen tras 1-2 horas. Además, incrementa el gasto cardíaco y disminuye la tolerancia al ejercicio. Estos efectos pueden aumentar el riesgo cardiovascular en personas con patología cardiaca o vascular previa [Sydney, 2002]. En estas últimas se han descrito algunos casos de arritmias graves [Jones, 2002; Sydney, 2002].
5.2.2. Efectos sobre el sistema respiratorio
El THC produce disminución en la resistencia de las vías aéreas y broncodilatación en personas sanas. Los efectos de fumar cannabis sobre el sistema respiratorio son los mismos que el consumo de tabaco. Si el cannabis se consume mezclada con tabaco, se está consumiendo tabaco y por ello se está expuesto al monóxido de carbono y las sustancias cancerígenas.
El consumo de «porros» produce incrementos superiores en la concentración de carboxihemoglobina que el tabaco puesto que se fuma sin filtro con inhalaciones largas y profundas y tiene una temperatura de combustión superior a la del tabaco. El consumo crónico de cannabis fumado se ha asociado a bronquitis y enfisema, y posiblemente podría incrementar el riesgo de carcinoma pulmonar [Ashton, 2001].
5.2.3. Efectos oculares
El cannabis produce enrojecimiento conjuntival como consecuencia de la vasodilatación, reducción de la producción de lágrimas, caída del párpado (ptosis palpebral), dificultad en la acomodación y disminución del reflejo pupilar a la luz. La administración local o sistémica produce una disminución marcada de la presión intraocular [Hollister, 1986].
5.2.4. Efectos gastrointestinales
El cannabis produce una reducción en la producción de saliva, sequedad de boca, reducción del peristaltismo intestinal y enlentecimiento del vaciado gástrico. El cannabis es antiemético (ver aplicaciones terapéuticas).
5.2.5. Efectos sobre la musculatura estriada
El cannabis produce relajación muscular. Además posee propiedades anticonvulsivantes en animales. Entre los distintos componentes del cannabis, parece que el cannabidiol sería el que posee mayor potencial anticonvulsivo
5.2.6. Efectos sobre el sistema inmunológico
Los datos sugieren que el THC puede ejercer efectos inmunomoduladores con acciones inhibidoras o estimulantes, dependiendo del sistema celular implicado y de la dosis utilizada. En consumidores recreativos de cannabis se ha observado una disminución de la inmunidad celular que se correlaciona con la historia de consumo de los sujetos [Pacifici y Cols, 2003]. No obstante, no existen evidencias claras de que el consumo de cannabis produzca alteraciones inmunológicas clínicamente significativas en humanos. Hasta la fecha no ha podido demostrarse que esta inmunosupresión pueda causar un mayor número de infecciones.
5.2.7. Efectos sobre el sistema endocrino y la conducta sexual
El THC disminuye la secreción de hormonas sexuales, con una reducción de la secreción de testosterona y del número y la motilidad de los espermatozoides. En mujeres, el consumo de cannabis produce una reducción del ciclo menstrual, niveles elevados de prolactina que pueden asociarse a la aparición de galactorrea, y niveles menores de andrógenos. Parece por todo ello que el THC podría reducir la fertilidad, aunque no ha podido demostrarse definitivamente [Brown and Dobs, 2002].
Como ocurre con la mayoría de drogas, los cannabinoides pueden afectar la conducta sexual con un resultado variable, que depende de la propia droga, la combinación con otras sustancias y el contexto de consumo. No se ha demostrado científicamente que el cannabis sea un afrodisíaco [Saso, 2002].
5.2.8. Embarazo
El consumo durante el embarazo en mujeres incrementa el riesgo para la madre, el feto y el neonato. El peso al nacer es menor, siendo un efecto dosis-dependiente. Los niños presentan alteraciones en las funciones cognitivas El THC atraviesa la barrera placentaria y se acumula en la leche materna, no recomendándose la lactancia materna en consumidoras de cannabis [House of Lords, 1998].
6. Efectos crónicos del cannabis
En consumidores habituales de cannabis se han descrito una serie de efectos que son los que se revisan en este apartado con la denominación de efectos crónicos. Sin embargo, antes de pasar a la revisión de los mismos deben realizarse una serie de consideraciones con el fin de enmarcar adecuadamente los resultados de los distintos estudios.
En primer lugar hay que resaltar que mientras que los efectos agudos del cannabis se han estudiado en condiciones de laboratorio en las que se ha dispuesto de los diseños y técnicas de investigación más adecuados para poder extraer conclusiones unívocas, en el caso de los efectos crónicos, los estudios se han llevado a cabo en diseños no experimentales. Los efectos del consumo crónico del cannabis se han extrapolado de los hallazgos de estudios de consumidores de cannabis a los que se ha seguido a lo largo de los años. Estos estudios adolecen de las limitaciones metodológicas comunes a todos los estudios naturalísticos: la existencia de factores genéticos, psicológicos y sociales previos al inicio del consumo de cannabis y comunes a los que pueden estar en la base de los efectos observados tras el consumo prolongado del cannabis y la imposibilidad de poder controlar de forma clara la cantidad y calidad de la exposición al tóxico.
En segundo lugar, hay que destacar que el consumo de cannabis suele realizarse de forma conjunta con otras sustancias (alcohol y tabaco principalmente), y es precisamente este patrón de policonsumo el que dificulta que pueda establecerse una asociación clara entre el consumo del cannabis y los efectos encontrados.
Tras estas consideraciones previas, a continuación se revisan algunos de los efectos que pueden aparecer tras el consumo repetido de cannabis y que son muy relevantes para el rendimiento escolar y psicomotor (Tabla 6).
TABLA 6. Efectos crónicos del cannabis

6.1. Efectos cognitivos y sobre el rendimiento psicomotor
El uso diario y durante periodos prolongados de cannabis puede producir deficiencias en la memoria, en la atención, la capacidad psicomotora y la velocidad de procesamiento de la información [Iversen, 2003].
Estas alteraciones psicológicas parecen relacionarse con cambios funcionales, del flujo sanguíneo y metabólicos en regiones prefrontales y cerebelares que se observan en estudios de neuroimagen en usuarios crónicos de cannabis [Pope y cols, 1995; Rogers y cols, 2001; Verdejo-García A y cols, 2004; Lundqvist 2005].
Se ha discutido si estos cambios son consecuencia del consumo crónico acumulado o de un estado de intoxicación aguda persistente tras un consumo diario. Los estudios más consistentes han demostrado que las alteraciones neurocognitivas descritas normalizan progresivamente si los individuos dejan de consumir, mejorando con el paso de los días. Parece que la afectación observada puede revertir casi en su totalidad a las 4 semanas de cesar el consumo de cannabis [Pope y cols, 2001; Solowij y cols, 2002; Pope y Cols, 2003]. Hay estudios que relacionan la persistencia de algunas alteraciones con el consumo de cannabis temprano (antes de los 17 años) [Pope y Cols, 2003].”
7. Cannabis y trastornos mentales
El consumo de cannabis puede dar lugar a una serie de trastornos mentales descritos en los principales sistemas internacionales de clasificación de las enfermedades: la Clasificación Internacional de Enfermedades, 10.ª revisión (CIE-10) [OMS, 1992] y el Manual Diagnóstico y Estadístico de los Trastornos Mentales, DSM-IV-TR [APA, 2000]. Además es frecuente la asociación entre el consumo de cannabis y otras enfermedades psiquiátricas entre las que destacan los trastornos de ansiedad y del estado de ánimo y, por su especial gravedad, los trastornos psicóticos (Tabla 8).
TABLA 8. Trastornos mentales relacionados y asociados con el consumo de cannabis
Trastornos por consumo de cannabis
• Dependencia
• Abuso
Trastornos asociados al consumo de cannabis
• Trastornos de ansiedad
• Trastornos depresivos
• Psicosis inducida y esquizofrenia
Otros cuadros clínicos relacionados con el consumo de cannabis
• Intoxicación
• Delirium
• Flashback
• «Síndrome amotivacional» o Intoxicación crónica
• Trastornos de personalidad
7.1. Trastornos por consumo de cannabis: Abuso y Dependencia
El consumo continuado de cannabis puede llevar hacia un consumo perjudicial o abuso y a la aparición de un trastorno por dependencia. La capacidad del cannabis para producir euforia o placer es el factor más determinante de su consumo. Este efecto reforzador se debe a la estimulación del sistema de recompensa límbico mediado por la dopamina y los opioides endógenos, resultando en un incremento de la liberación de dopamina en el núcleo accumbens, al igual que producen otras drogas reforzadoras como la heroína, anfetaminas, cocaína y la nicotina. Se ha descrito el desarrollo de tolerancia farmacológica y síndrome de abstinencia en humanos con el consumo continuado de cannabis. La tolerancia parece ser debida a la disminución de la sensibilidad o del número de los receptores CB1 [De Fonseca et al., 1994] y su desarrollo facilita la escalada de la dosis o el incremento en la frecuencia del consumo que se observa en los estudios longitudinales de consumidores [Swift et al., 2000].
Las manifestaciones iniciales del trastorno por abuso de cannabis consisten en abandono del grupo de amigos no consumidores, desinterés por actividades que no tengan relación directa con el consumo y preocupación por disponer de cannabis. Cuando estas situaciones se acompañan además del uso compulsivo de la sustancia se denomina ya trastorno por dependencia. El problema se detecta inicialmente por familiares, profesores o amigos, y el individuo no acostumbra a relacionar las alteraciones cognitivas con el consumo. En otras ocasiones, son las personas los que acuden solicitando tratamiento después de algún fracaso a nivel escolar, laboral o por molestias físicas. El trastorno puede ir acompañado de un síndrome de abstinencia caracterizado por irritabilidad, agresividad, inquietud, nerviosismo, ansiedad, disminución o pérdida del apetito y dificultades para dormir, incluyendo la presencia de sueños extraños, que mejoran con el consumo de cannabis [Budney et al., 2004] (Tabla 9). Este síndrome puede aparecer a los 3-7 días de cesar el consumo y suele resolverse pasados unos 28 días [Ashton, 2001].
TABLA 9. Clínica del abuso o dependencia de cannabis
• Abandono del grupo de amigos no consumidores
• Desinterés por actividades que no tengan relación directa con el consumo
• Preocupación por disponer de cannabis
• Uso compulsivo del cannabis
• Problemas de rendimiento escolar o laboral
• Síntomas de abstinencia caracterizados por: Irritabilidad, agresividad, inquietud, nerviosismo, disminución del apetito, y dificultades para dormir, que ceden alconsumir cannabis
Se estima que entre 7 y 10% de los que han probado el cannabis tienen riesgo de desarrollar un trastorno de dependencia [Hall y Solowij, 1998]. La aparición de ésta depende fundamentalmente del patrón de consumo, observándose que a mayor frecuencia de consumo, mayor riesgo de desarrollarla (desde 1 de cada 10 en consumidores ocasionales, hasta 1 de cada 3 en consumidores frecuentes), y de la concentración de THC en los derivados del cannabis consumidos (a mayor concentración de THC mayor riego de desarrollar dependencia) [Chait y Burke, 1994]. Otros factores predictores de la aparición de dependencia de cannabis son ser hombre, con conductas antisociales y ser fumador de tabaco [Coffey et al., 2003].
7.2. Trastornos de ansiedad y consumo de cannabis
Los trastornos de ansiedad junto con los depresivos, son las complicaciones psiquiátricas más frecuentes asociadas al consumo de cannabis. La sintomatología ansiosa suele asociarse a la intoxicación aguda y en muchos casos se desencadena por la presencia de ideas paranoides. La prevalencia de aparición de sintomatología ansiosa puede llegar al 22%, depende de la dosis y se da con mayor frecuencia en consumidores poco experimentados y en mujeres [Thomas, 1996].
7.3. Trastornos del estado de ánimo y consumo de cannabis
En estudios longitudinales llevados a cabo en población general, se ha observado una modesta asociación entre depresión y consumo importante de cannabis, que desaparece cuando los consumos de cannabis son poco frecuentes. Así mismo parece haber una pequeña asociación entre inicio temprano, consumo regular de cannabis y aparición posterior de depresión. A la inversa, hay escasa evidencia de que los sujetos con depresión presenten un riesgo elevado de consumir cannabis posteriormente. Con los datos actuales no se puede descartar que la asociación entre cannabis y depresión sea debida a factores sociales, familiares y ambientales comunes que aumentan el riesgo tanto del consumo importante de cannabis como de la depresión [Degenhardt et al., 2003a]. En algunos estudios se ha descrito más falta de interés (anhedonia), ideación suicida e intentos de suicidio entre los consumidores de cannabis [Beautris et al., 1999; Bovasso et al., 2001; Patton et al., 2002].
7.4. Consumo de cannabis y psicosis
La relación entre el consumo de cannabis y la psicosis es uno de los temas de discusión más candentes en la actualidad debido a la elevada prevalencia del consumo de cannabis y a la gravedad clínica propia de la psicosis. Con los conocimientos disponibles podemos afirmar que:
a) La intoxicación aguda por cannabis puede producir síntomas psicóticos tales como despersonalización, desrealización, sensación de pérdida de control e ideas paranoides.
b) El consumo de cannabis puede originar psicosis inducidas, de corta duración y que ceden con la abstinencia prolongada.
c) El consumo de cannabis es muy prevalente en sujetos con trastornos mentales graves como la esquizofrenia.
El punto clave está en la naturaleza de la asociación del consumo de cannabis y la aparición de psicosis. Algunos autores apuntan a que el consumo de cannabis precipita psicosis en sujetos vulnerables, mientras que otros estudios defienden que esta relación es debida a factores de confusión no controlados o a que el cannabis es utilizado para automedicar los síntomas de la psicosis incipiente.
Actualmente disponemos de varias revisiones sistemáticas de los estudios publicados sobre la asociación entre consumo de cannabis y psicosis [Arsenault et al., 2004; McLeod et al., 2004; Smit et al., 2004; Semple et al., 2005; Henquet et al., 2005a]. Globalmente estos estudios muestran que el consumo de cannabis puede aumentar en 2-3 veces el riesgo de aparición psicosis a lo largo de la vida (Tabla 10).
Cuando se estudia la relación de causalidad de esta asociación, la mayoría de los estudios sugieren que el consumo de cannabis lleva a la aparición de la psicosis [Van Os, et al., 2002; Arsenault et al., 2002; Stefanis et al., 2004; Fergusson et al., 2005], aunque otros han demostrado que sujetos potencialmente psicóticos tienen mayor probabilidad de consumir cannabis, sugiriendo también que la psicosis puede predisponer al consumo de cannabis [Henquet et al., 2005b; Ferdinand et al., 2005]. Esta relación bidireccional entre factor de riesgo y enfermedad es frecuente en las enfermedades psiquiátricas como la psicosis. Independientemente de la dirección de la relación, la coexistencia de consumo de cannabis y psicosis aumenta la gravedad del cuadro clínico.
Tabla 10. Asociación entre consumo de cannabis y psicosis: revisiones sistemáticas y meta-análisis

Los resultados de los estudios permiten afirmar que hay una relación de causa-efecto entre consumo de cannabis y aparición posterior de psicosis, que esta relación depende de la dosis (a mayor consumo de cannabis, mayor es el riesgo de psicosis), que el consumo de cannabis suele preceder a la aparición de la psicosis, y que el consumo de cannabis al principio de la adolescencia aumenta el riesgo de psicosis posterior [Henquet et al., 2005b].
Se han descrito una serie de mecanismos biológicos que pueden explicar esta asociación. Los más probables implican los efectos del THC en la regulación de la dopamina en el cerebro. La hipótesis dopaminérgica de la esquizofrenia propone que los síntomas psicóticos están causados, al menos en parte, por un aumento en la transmisión dopaminérgica por las terminales nerviosas que proyectan en el sistema límbico y en el neocortex. Hay evidencias de que la estimulación de los receptores cannabinoides por el THC pueden aumentar la liberación de dopamina [Cheer et al., 2004]. Estudios en experimentación animal han observado que el tratamiento cannabinoide crónico durante la pubertad induce cambios conductuales y cognitivos que no se encuentran si la exposición ocurre en animales adultos [Schneider et al., 2003]. Estos hallazgos pueden estar en las bases neurobiológicas de los trastornos psicóticos, pudiendo determinar el riesgo de aparición de estos trastornos en los adultos [Veen et al., 2004]. Otro mecanismo implicado puede ser la sensibilización dopaminérgica inducida por el consumo regular de cannabis, en la que los sujetos se hacen progresivamente más vulnerables a las alteraciones cognitivas y perceptivas inducidas por la dopamina y progresan a síntomas psicóticos completos [Howes et al., 2004]. En general se puede afirmar que los estudios neurobiológicos sobre los efectos del cannabis en el SNC sugieren claramente que esta sustancia afecta el sistema dopaminérgico, el cual tiene un papel clave en el desarrollo de los síntomas psicóticos [Fergusson et al., 2006].
Sin embargo, puesto que no todos los sujetos con psicosis han estado expuestos al cannabis y no todos los consumidores de cannabis desarrollan psicosis, el cannabis no es una causa necesaria ni suficiente, sino que actúa sobre otros factores para tener una influencia causal sobre el riesgo de psicosis [Degenhardt & Hall, 2002; Degenhardt et al., 2003b]. Diversos estudios sugieren que el factor con el que el cannabis puede combinarse para ejercer la influencia causal es la vulnerabilidad genética del individuo para la psicosis. En este sentido, disponemos de diversas pruebas indirectas de este riesgo genético: mayor frecuencia de esquizofrenia en los familiares de los pacientes con psicosis aguda que consumen cannabis, que en los que no lo consumen [McGuire et al., 1995]; mayor frecuencia de experiencias psicóticas tras el consumo de cannabis en sujetos con propensión a la psicosis [Verdoux et al., 2003; Henquet et al., 2005b] y una mayor sensibillidad de los pacientes con esquizofrenia a las alteraciones cognitivas inducidas por el cannabis [D’Souza et al., 2005]. El resultado de algunos estudios avalan esta predisposición genética [Caspi et al., 2005]. Así pues, con los datos disponibles se puede afirmar la asociación entre el consumo de cannabis y la aparición de psicosis se explica por un mecanismo de interacción genambiente.
Esta interacción entre el consumo de cannabis y la vulnerabilidad explicaría porque el riesgo de psicosis en los consumidores de cannabis sólo es 2-3 veces superior que en los no consumidores; por qué no se han detectado grandes incrementos en la incidencia de psicosis en consonancia con el aumento en las tasas de consumo de cannabis en los adolescentes en las últimas décadas, y por qué la edad de inicio de la psicosis es más precoz en los consumidores de cannabis [Arendt et al., 2005; Veen et al., 2004].
Así pues, aunque no se puedan descartar totalmente algunos factores de confusión no controlados, con las pruebas disponibles se impone la aplicación del principio de precaución y desde la perspectiva de salud publica debe recomendarse que los adolescentes no consuman cannabis [De Irala et al., 2005]. Debe transmitirse a los jóvenes la idea de que el consumo de cannabis puede aumentar el riesgo de desarrollar una esquizofrenia (desde 0.7/1000 al 1.4/1000 habitantes). Este riesgo es probablemente mayor en los que son vulnerables en un sentido todavía difícil de especificar más allá de una historia familiar de psicosis o una historia personal de sensaciones y vivencias extravagantes [Hall, 2006].
7.5. Otros cuadros clínicos relacionados con el consumo de cannabis
7.5.1. Delírium por intoxicación por cannabis.
Aunque no es frecuente, cuando el cannabis se consume en grandes cantidades puede producir un cuadro de delirium. Los síntomas típicos son confusión, alteraciones de la memoria, sensación de temor, suspicacia, despersonalización, desrealización y alteraciones sensoperceptivas. La psicopatología de estas reacciones es indistinguible de los cuadros de delírium de otra etiología. Son cuadros clínicos transitorios y limitados en el tiempo, pero recurrentes en sucesivas exposiciones al tóxico. Este cuadro también puede aparecer en sujetos que consumen el cannabis por primera vez [Tunving, 1985].
7.5.2. Flashbacks por cannabis
Se refiere a la aparición de vivencias-alucinaciones con la cualidad de una percepción real (las mismas experiencias que sintió la persona cuando había consumido el tóxico), después de semanas o meses de abstinencia. Aunque son más comunes en personas que han consumido drogas alucinógenas pero también se han descrito de forma ocasional en consumidores de cannabis [Tunving, 1985; Johns, 2001; Poole y Brabbins, 1996].
7.5.3. Cannabis y síndrome amotivacional
En consumidores de cannabis a dosis elevadas y durante un tiempo prolongado se ha descrito el llamado «síndrome amotivacional», que estaría caracterizado por un deterioro en la personalidad del sujeto, pérdida de energía y abulia con importante limitación de las actividades habituales. La sintomatología desaparece tras la abstinencia prolongada de la sustancia [Thomas, 1993]. La validez de este diagnóstico permanece incierta y actualmente se considera que probablemente corresponde a la sintomatología propia de la intoxicación crónica en consumidores frecuentes. También puede estar relacionado con rasgos de personalidad en un subgrupo de consumidores de esta sustancia [Johns, 2001; Negrete et al., 1986].
7.5.4. Trastornos de personalidad
Al igual que sucede con el resto de las dependencias a drogas ilegales, el trastorno de personalidad antisocial en el adulto y el trastorno disocial en el adolescente, son los que han mostrado una mayor asociación con el trastorno por dependencia del cannabis [Agosti et al., 2002], aunque en el caso del cannabis, el trastorno de personalidad esquizotípico es el que despertado mayor interés por su relación con la aparición de síntomas psicóticos [Mass et al., 2001].
8. Tratamiento de la dependencia de cannabis
Con la salvedad del incremento en el número de demandas de tratamiento por cannabis en los adolescentes, en general se observa que la proporción de los sujetos que acuden en demanda de tratamiento por el consumo de cannabis es muy baja si tenemos en cuenta el elevado número de sujetos con consumo problemático de esta sustancia. Esta escasa demanda de tratamiento puede explicarse por distintas razones.
En primer lugar destaca la percepción generalizada, en el sujeto consumidor, de que el cannabis es una droga relativamente inocua. Inicialmente el problema es detectado por familiares, profesores o amigos mientras que el individuo no acostumbra a relacionar las alteraciones cognitivas con el consumo. Menos veces, son los sujetos los que acuden en demanda de tratamiento por su incapacidad para controlar o interrumpir el consumo, a pesar de los problemas escolares o laborales o por el aumento de irritabilidad, conducta agresiva, depresión nerviosismo y ansia de consumo. Los pacientes que acuden a tratamiento por el cannabis suelen ser hombres (70%) y fumadores de cannabis varias veces por semana. Los motivos de solicitar tratamiento suelen estar relacionados con la pérdida de motivación (84%) y las sensaciones paranoides (78%), detectándose además en muchos casos problemas respiratorios (86%) [Copeland et al., 2001a].
En segundo lugar destaca la resistencia de los pacientes a participar en programas de tratamiento en los que la mayoría de sujetos son dependientes de alcohol, heroína y cocaína y en los que no se oferta terapias específicas para cannabis [Marijuana Treatment Project Research Group, 2004; Weiner et al., 1999].
Actualmente se propone aplicar al tratamiento de la dependencia del cannabis los criterios que se aplican al tratamiento de la dependencia de cualquier droga: desintoxicación seguida de deshabituación.
8.1. Tratamiento de desintoxicación
La desintoxicación es el primer paso para el tratamiento de un trastorno por dependencia de una droga. Esta dirigida a paliar el cuadro clínico que aparece cuando de forma brusca deja de consumirse la sustancia (síndrome de abstinencia). Se realiza con medicación y basándose en la propiedad farmacológica de la tolerancia cruzada. Para algunas drogas (por ejemplo, la heroína), existen tratamientos específicos para la desintoxicación (por ejemplo la metadona), mientras que para otras, entre las que se encuentra el cannabis, en la actualidad no hay ningún tratamiento farmacológico específico. Por lo tanto debe realizarse un tratamiento sintomático [Haney 2005].
8.2. Tratamiento de deshabituación
El tratamiento de deshabituación se refiere a la fase de tratamiento que se realiza después de la desintoxicación y que esta dirigida a mantener la abstinencia en la sustancia y evitar la recaída en el consumo. En tanto que las adicciones son enfermedades crónicas y recidivantes, el tratamiento de deshabituación es fundamental para conseguir la abstinencia a largo plazo. Los tratamientos propuestos para la deshabituación del abuso de cannabis son psicológicos y farmacológicos.
8.2.1. Tratamientos psicológicos
Los tratamientos psicológicos son los habituales en el tratamiento de las drogodependencias: psicoterapia de orientación cognitivo conductual, psicoterapia motivacional y terapia de incentivos [Marijuana Treatment Project Research Group; 2004; Budney et al., 2000; Stephens et al., 1994; 2000; Copeland et al., 2001b]. Globalmente los resultados de los distintos estudios realizados con las diversas modalidades de psicoterapia comparadas entre si y con grupos control sin tratamiento, sugieren que las distintas psicoterapias son eficaces, aunque el principal problema, común a todas, es la falta de adhesión al tratamiento.
8.2.2. Tratamientos farmacológicos
Hasta la actualidad no disponemos de ningún fármaco que haya demostrado su eficacia en el tratamiento de deshabituación de la dependencia de cannabis. Se están realizando diversos estudios experimentales cuyos resultados pueden aportar nuevas estrategias farmacológicas [Haney et al., 2005].
Por lo tanto, el tratamiento del abuso y dependencia de cannabis debe combinar la terapia psicológica y el tratamiento farmacológico sintomático.
[…]
10 . Posibles usos terapéuticos de los cannabinoides
Además de los usos recreacionales, el cannabis se ha utilizado de forma empírica desde la antigüedad por sus supuestas propiedades terapéuticas. En los últimos años se ha descrito su consumo por parte de grupos de pacientes en algunas enfermedades y se ha investigado su posible utilidad en diferentes indicaciones.
El potencial terapéutico del cannabis ha sido revisado ampliamente en numerosas publicaciones científicas [Grotenhermen et al., 2003; Guy et al., 2004; Duran et al., 2004; Abanades et al., 2005] y por organismos como el Comité Científico de la Cámara de los Lores Británica [House of Lords, 1998 o el Institute of Medicine norteamericano, 1999].
La indicación en la que existen más evidencias es en la prevención y tratamiento de la nauseas y vómitos secundarios al tratamiento con antineoplásicos. También hay evidencias basadas en los resultados de ensayos clínicos aleatorizados y controlados en el tratamiento de la pérdida de apetito del síndrome de anorexia y caquexia (SIDA y cáncer terminal), en la esclerosis múltiple; tratamiento del dolor neuropático, control de la espasticidad muscular y otros síntomas, o en el tratamiento del dolor neuropático de otras etiologías.
En la tabla 11 se presentan las únicas indicaciones médicas aprobadas para la prescripción de algunos de los derivados del cannabis (naturales o sintéticos) en este momento [Abanades et al., 2005]. En general los preparados descritos no son el tratamiento de elección de estas patologías. Los cannabinoides son una alternativa a emplear en el caso de que no se observe respuesta a otros fármacos. En general no se consideran medicamentos de primera línea de tratamiento.
Como ocurre con la mayoría de medicamentos, el uso terapéutico de los cannabinoides precisa de la intervención de un médico para realizar el diagnóstico, seleccionar el tratamiento y prescribir el que se ajuste mejor a las necesidades del paciente y hacer el seguimiento de la eficacia así como de la toxicidad del medicamento y la evolución de la enfermedad.
TABLA 11. Cannabis y derivados: Indicaciones aprobadas actualmente

(1) Dronabinol (Marinol®): comprimidos de delta-9-tetrahidrocannabinol (THC) sintético.
(2) Nabilona (Cesamet®): cápsulas del análogo sintético del delta-9-tetrahidrocannabinol (THC).
(3) Sativex®: spray para uso en mucosa oral de delta-9-tetrahidrocannabinol (THC) 27mg/ml y cannabidiol (CBD) 25mg/ml. Procedente de extracto de Cannabis sativa L.
11. Conclusiones
a) El cannabis es la droga ilegal más consumida en todo el mundo y tanto en la Unión Europea como en España, su consumo está aumentandoa lo largo de los últimos años con una tendencia creciente.
b) El consumo de cannabis, junto con el de alcohol y tabaco, forma parte de los hábitos y estilos de vida de una proporción importantede jóvenes. Estos consumos, junto a la baja percepción de riesgo de los mismos y a una mayor disponibilidad para conseguir estas sustancias, hacen que el cannabis se haya convertido en una droga de uso recreativo asociada al tiempo de ocio de los jóvenes que banalizan su consumo.
c) Aunque el cannabis sea la primera droga ilegal consumida y existan estudios que sugieren que puede actuar como facilitadora de otras sustancias, ello no significa que todos los que la consumen acaben consumiendo otras drogas.
d) El inicio precoz del consumo de cannabis, aumenta el riesgo de la presencia de problemas relacionados con su consumo, tanto en la esfera escolar, como en la social y de trastornos mentales.
e) El consumo de cannabis en el periodo académico se asocia a peores notas, menor satisfacción, actitudes negativas hacia la escuela, pobre rendimiento escolar, aumento del absentismo y mayor prevalencia de abandono de los estudios.
f) El consumo de cannabis produce alteraciones a nivel del SNC y de otros órganos y sistemas, siendo éstas de peor pronóstico cuando el consumo es precoz.
g) El uso diario y durante periodos prolongados de cannabis puede producir deficiencias en la memoria, la atención, la capacidad psicomotora y otros trastornos mentales.
h) El cannabis es una droga y como tal se comporta, su consumo continuado puede llevar al abuso o la dependencia.
i) El consumo de cannabis puede triplicar el riesgo de aparición de psicosis sobre todo en sujetos vulnerables.
j) Se observa que la proporción de sujetos que acuden en demanda de tratamiento por el consumo de cannabis es muy baja si tenemos en cuenta el elevado número de sujetos con consumo problemático de esta sustancia.
12. Bibliografía
Abanades S, Cabrero A, Fiz J, Farré M.: Farmacología clínica del cannabis
2005;20:187-98.
Agosti, V., Nunes, E., & Levin, F. (2002). Rates of psychiatric comorbidity among US residents with lifetime cannabis dependence. American Journal of Drug and Alcohol Abuse, 28 645-654.
Aharonovich, E., Liu, X., Nunes, E., Waxman, R. and Hasin, D.: Postdischarge cannabis use and its relationship to cocaine, alcohol, and heroin use: a prospective study. Am J Psychiatry 2005; 162: 1507-1514.
Ahston CH. Pharmacology and effects of cannabis: a brief review. Br J Psychiatry 2001; 178: 101-106.
American Psychiatric Association. DSM-IV, Diagnostic and Statistical Manual of Mental Disorders. 4th Edition-TR. American Psychiatric Association 2000. Washington, DC.
Arendt M, Rosenberg R, Foldager L, Perto G, Munk-Jorgensen P. Cannabis-induced psychosis and subsequent schizophrenia-spectrum disorders: followup study of 535 incident cases. Br J Psychiatry 2005; 187:510-15.
Arseneault L, Cannon M, Poulton R, Murray R, Caspi A, Moffitt TE. Cannabis use in adolescence and risk for adult psychosis: longitudinal prospective study. Brit Med J. 2002; 325(7374):1212-1213.
Arseneault L, Cannon M, Witton J, Murray R. Causal association between cannabis and psychosis: examination of the evidence. Br J Psychiatry, 2004; 184: 110-17.
Ashton CH. Pharmacology and effects of cannabis: a brief review. Br J Psychiatry. 2001;178:101-6.
Beautrais AL, Joyce PR, Mulder RT. Cannabis abuse and serious suicide attempts. Addiction 1999; 94: 1155-1164.
Blows S, Ivers RQ, Connor J, Ameratunga S, Wodward M, Norton R. Marijuana use and car crash injury. Addiction 2005; 100: 605-611.
Bogenschutz, MP: Drug Information Libraries on the Internet. J of Psychoactive Drugs 2000; 32: 249-258.
Bovasso GB. Cannabis abuse as a risk factor for depressive symptoms. Am J Psychiatry 2001;158:2033-7.
Boyer EW, Woolf A: What’s New on the Street? Clinical Pediatric Emergency Medicine 2000;1:13-17.
Boys A, Farrell M, Taylor C, et al. Psychiatric morbidity and substance use in young people aged 13-15 years: Results from the Child and Adolescent Survey of Mental Health. Br JPsychiatry 2003;182:509-17.
Brown TT, Dobs AS. Endocrine Effects of Marijuana. J Clin Pharmacol 2002; 2002;42:90S-96S.
Budney AJ, Higgins ST, Radonovich KJ, Novy PL: Adding voucher-based incentives to coping skills and motivational enhancement improves outcomes during treatment for marijuana dependence. J Consult Clin Psych 2000, 68:1051-1061.
Budney AJ, Hughes JR, Moore BA, Vandrey R. Review of the validity and significance of cannabis withdrawal syndrome. Am J Psychiatry 2004; 161:1967-1977.
Camí J, Guerra D, Ugena B, Segura J, de la Torre R. Effect of subject expectancy on the THC intoxication and disposition from smoked hashish cigarettes. Pharmacol Biochem Behav. 1991;40:115-9.
Caspari D. Cannabis and schizophrenia: results of a follow-up study. Eur Arch Psychiatry Clin Neurosci 1999; 249: 45-49.
Caspi A, Moffitt TE, Cannon M, et al. Moderation of the effect of adolescent onset cannabis use on adult psychosis by a functional polymorphism in the catechol- Omethyltransferase gene: longitudinal evidence of a gene 3 environment interaction. Biol Psychiat 2005;57(10): 1117-1127.
Cheer JF, Wassum K, Hein M, Phillips P, Wightman R. cannabinoids enhance subsecond dopamine rlease in the nucleo accumbens of awake rats. J Neuroscience 2004; 24: 4393-400.
Coffey C, Carlin JB, Lynskey M, Li N, Patton GC. Adolescent precursors of cannabis dependence: findings from the Victorian Adolescent Health Cohort Study. Br J Psychiatry. 2003 Apr;182:330-6.
Copeland J, Swift W, Rees V. Clinical profile of participants in a brief intervention program for cannabis use disorders. J Subst Abuse Treat 2001; 20: 45-52. (a).
Copeland J, Swift W, Roffman R, Stephens R: A randomized controlled trial of brief cognitive-behavioral interventions for cannabis use disorder. J Subst Abuse Treat 2001, 21:55-64. (b).
Chait LD, Burke KA, Preference for high-versus low-potency marijuana. Pharmacol Biochem Behav 1994; 49: 643-647.
De Fonseca FR, Gorriti MA, Fernandez-Ruiz JJ, Palomo T, Ramos JA. Down regulation of rat brain cannabionoid sites after chronic -9- tetrahydrocannabinol treatment. Pharmacol Biochem Behav 1994; 47: 33-40.
De Fonseca FR, Carrera MRA, Navarro M, Koob GF, Weiss F. Activation of corticotrophin releasing factor in the limbic system during cannabinoid withdrawal. Science 1997; 276: 2050-2054.
De Irala J, Ruiz-Canela M, martínez-González MA. Causal relationship between cannabis use and psychotic symptoms or depression. Should we wait and see? A public health perspective. Med Sci Monit 2005; 11: RA355-358.
Degenhardt L, Hall W, Lysnkey M. The relationships between cannabis use and other substance use in the general population. Drug Alcohol Depend 2001; 64: 319-327.
Degenhardt L, Hall W. Cannabis and psychosis. Curr Psychiatry Rep 2002; 4(3):191-196.
Degenhardt L, Hall W, Lynskey M. Exploring the association between cannabis use and depression. Addiction. 2003 Nov;98(11):1493-504 (a).
Degenhardt L, Hall W, Lynskey M. Testing hypotheses about the relationship between cannabis use and psychosis. Drug Alcohol Depen 2003;71(1):37-48.(b).
DeWit DJ, Offord DR, Wong M. Patterns of onset and cessation of drug use over the early part of the life course. Health Educ Behav. 1997 Dec;24(6):746-58.
D’Souza DC, Abi-Saab WM, Madonick S, et al. Delta-9-tetrahydrocannabinol effects in schizophrenia: implications for cognition, psychosis, and addiction. Biol Psychiat 2005; 57(6):594-608.
Duran M, Laporte JR, Capella D. Novedades sobre las potencialidades terapéuticas del cannabis y el sistema cannabinoide. Med Clin (Barc). 2004;122:390-8.
Ehrenreich H, Rinn T, Kunert HJ, Moeller MR, Poser W., Schilling L, Gigerenzer G, Hoeche MR. Specific attentional dysfunction in adults followingearly start of cannabis use. Psychopharmacology. 1999 Mar;142(3):295-301.
European Monitoring Centre for Drugs and Drug Addiction (EMCDDA). An overview of cannabis potency in Europe. EMCDDA Insights. Luxembourg: Office fro Official Publications of the Europena Communities; 2004.
Falck RS, Carlson RG, Wang J, Siegal HA: Sources of information about MDMA (3,4-methylenedioxymethamphetamine): perceived accuracy, importance, and implications for prevention among young adult users. Drug Alcohol Depend 2004;74:45-54.
Flash Eurobarometer 158: Young People and Drugs. European Commission, 2004 [consultado 12 jul 2005]. Disponible en: http://europa.eu.int/comm/public_opinion/flash/fl158_en.pdf.
Ferdinand RF, Sondeijker F, Van der Ende J, Selten JP, Huizink A, Verhulst FC. Cannabis use predicts future psychoticsymptoms; and vice versa. Addiction 2005;100(5):612-618.
Fergusson DM, Horwood LJ. Early onset cannabis use and psychosocial adjustment in young adults. Addiction. 1997;92:279-96.
Fergusson DM, Horwood LJ. Does cannabis use encourage other forms of illicit drug use? Addiction 2000;95:505-20.
Fergusson DM, Horwood LJ, Swain-Campbell N. Cannabis use and psychosocial adjustment in adolescence and young adulthood. Addiction. 2002;97: 1123-35.
Fergusson DM, Horwood LJ, Swain-Campbell NR. Cannabis dependence and psychotic symptoms in young people. Psychol Med 2003;33(1):15-21.
Fergusson DM, Horwood LJ, Ridder EM. Tests of causal linkages between cannabis use and psychotic symptoms. Addiction 2005;100(3):354-366.
Fergusson DM, Poulton R, Smith PF, Boden JM. Cannabis and psychosis. BMJ 2006; 332: 172-174.
Gardner EL. Cannabinoid interaction with reward systems. En: Nahas GG, Sutin KM, Harvey DJ, Agurell S (eds). Marihuana and medicine. Totowa NJ: Humana Press, 1999; 187-205.
Grant BF, Dawson DA. Age of onset of drug use and its association with DSMIV drug abuse and dependence: results from the National Longitudinal Alcohol Epidemiologic Survey. J Subst Abuse. 1998;10(2):163-73.
Grotenhermen F., Russo E., Navarrete R editores. Cannabis y cannabinoides, farmacología, toxicología y potencial terapéutico. Sevilla: Castellarte; 2003.
Grotenhermen F. Pharmacokinetics and pharmacodynamics of cannabinoids. Clin Pharmacokinet. 2003;42:327-60.
Guy GW, Whittle BA and Robson PJ. Editores. The medicinal uses of cannabis and cannabinoids. London. Pharmaceutical Press 2004.
Hall W, Solowij N. Adverse effects of cannabis. Lancet 1998; 352: 1611-1616.
Hall et al. The health and psychological effects of cannabis use. Monograph Series N.º 44. Commonwealth of Australia, 2001 [consultado 22 jun 2005]. Disponible en: http://www7.health.gov.au/pubhlth/publicat/document/mono44.pdf.
Hall WD, Lynskey M. Is cannabis a gateway drug?. Testing hypothesis about the relationship between cannabis use and the use of other illicit drugs. Drug Alcool Rev 2005; 24: 39-48.
Hall W. Is cannabis use psychotogenic?. Lancet 2006; 367: 193-195.
Halpern JH, Pope HG: Hallucinogens on the Internet: a vast new source of underground drug information. Am J Psychiatry 2001;158:481-483.
Haney M. The marijuana withdrawal syndrome: diagnosis and treatment. Current Psychaitry reports 2005;7:360-6.
Hart CL, Ward AS, Haney M, Comer SD, Foltin RW, Fischman MW. Comparison of smoked marijuana and oral Delta(9)-tetrahydrocannabinol in humans. Psychopharmacology (Berl). 2002;164:407-15.
Hart CL. Increasing treatment options for cannabis dependence: a review of potential pharmacotherapies. Drug Alcohol Depend 2005; 80: 147-159.
Henquet C, Murray R, Linszen D, van Os J. The environment and schizophrenia: the role of cannabis use. Schizophr Bull. 2005 Jul;31(3):608-12. (a).
Henquet C, Krabbendam L, Spauwen J, et al. Prospective cohort study of cannabis use, predisposition for psychosis, and psychotic symptoms in young people. Brit Med J 2005;330(7481):11. (b).
Hibell B, Andersson B, Bjarnasson T et al. (2004): The ESPAD Report 2003: Alcohol and other drug use among students in 35 European Countries, Consejo Sueco de Información sobre Alcohol y otras Drogas (CAN) y Grupo Pompidou del Consejo de Europa.
Hollister LE. Health aspects of cannabis. Pharmacol Rev. 1986;38:1-20.
House of Lords Select Committee on Science and Technology. Cannabis: The Scientific and Medical Evidence. London: House of Lords, The Stationary Office, 1998 —consultado 5 jul 2005—. Disponible en: http://www.parliament.the-stationery-office.co.uk/pa/ld199798/ldselect/ldsctech/151/15101.htm.
Howes OD, McDonald C, Cannon M, Arseneault L, Boydell J, Murray RM. Pathways to schizophrenia: the impact of environmental factors. Int J Neuropsychoph 2004;7:(suppl)(1) S7-S13.
Howlett AC, Breivogel CS, Childers SR, Deadwyler SA, Hampson RE, Porrino LJ. Cannabinoid physiology and pharmacology: 30 years of progress. Neuropharmacology. 2004;47 Suppl 1:345-58.
Huestis M.A. Pharmacokinetics and Metabolism of the Plant Cannabinoids, D-9-THC, Cannabidiol and Cannabinol. En: Pertwee R, editor. Cannabinoids. Germany:Springer; 2005. p.657-690.
Institute of Medicine. Marijuana and Medicine: Assessing the Science Base. Washington, DC: National Academy Press, 1999.
Iversen L. Cannabis and the brain. Brain. 2003; 126:1252-70.
Johns A. Psychiatric effects of cannabis. Br J Psychiatry 2001; 178: 116-122.
Jones RT. Cardiovascular system effects of marijuana. J Clin Pharmacol 2002; 42:58S-63S.
Laumon B, Gadegbeku B, Martin JL, Biecheler MB. Cannabis intoxication and fatal road crashes in France: population based case-control study. British Medical Journal 2005; 331: 1371-1376.
Levin FR, McDowell D, Evans SM, Nunes E, Akerele E, Donovan S, Vosburg SK. Pharmacotherapy for marijuana dependence: a double-blind, placebo-controlled pilot study of divalproex sodium. Am J Addict. 2004 Jan-Feb;13(1):21-32.
Lundqvist T. Cognitive consequences of cannabis use: Comparison with abuse of stimulants and heroin with regard to attention, memory and executive functions. Pharmacol Biochem Behav. 2005;81:319-30.
Lynskey MT, Heath AC, Bucholz KK, Slutske WS, Madden PA, Nelson EC, Statham DJ, Martin NG. Escalation of drug use in early-onset cannabis users vs co-twin controls.JAMA. 2003 Jan 22-29;289(4):427-33.
Lynskey MT, Glowinski AL, Todorov AA, Bucholz KK, Madden PA, Nelson EC, Statham DJ, Martin NG, Heath AC. Major depressive disorder, suicidal ideation, and suicide attempt in twins discordant for cannabis dependence and earlyonset cannabis use. Arch Gen Psychiatry. 2004 Oct;61(10):1026-32.
Macleod J, Oakes R, Copello A, Crome I, Egger M, Hickman M, Oppenkowski T, Stokes-Lampard H, Davey Smith G. Psychological and social sequelae of cannabis and other illicit drug use by young people: a systematic review of longitudinal, general population studies. Lancet. 2004;363:1579-88.
Mann R, Brands B, Macdonald S, Stoduto G. Impacts of cannabis on driving: An analysis of current evidence with an emphasis on Canadian data. Ontario: Road Safety and Motor Vehicle Regulation, 2003.
Manzanares J, Corchero J, Romero, Fernández-Ruiz JJ, Ramos JA, Fuentes JA. Pharmacological and biochemical interactions between opioids and cannabinoids. Trends Pharmacol Sci 1999; 20: 287-293.
Marijuana Treatment Project Research Group; Brief treatments for cannabis dependence: findings from a randomized multisite trial. J Consult Clin Psychology 2004; 72: 455-466.
Mass R, Bardong C, Kindl K, Dalaume B. Relationship between cannabis use, schizotypal traits, and cognitive function in healthy subjects. Psychopathology 2001; 34: 209.14.
McGuire PK, Jones P, Harvey I, Williams M, McGuffin P, Murray RM. Morbid risk of schizophrenia for relatives of patients with cannabis-associated psychosis. Schizophr Res 1995;15(3):277-281.
Moore BA, Budney AJ. Relapse in outpatient treatment for marijuana dependence. J Subst Abuse Treat 2001; 21: 55-64.
Morral, A.R., McCaffrey, D.F., Paddock, S.M. Reassessing the marijuana gateway effect. Addiction 2002; 97: 1493-1504.
Negrete JC, Knapp WP, Douglas DE, Smith WB. Cannabis affects the severity of schizophrenic symptoms: results of a clinical survey. Psychol Med 1986; 16: 515-520.
Observatorio Español sobre Drogas (OED). Informe 2004: Situación y tendencias de los problemas de drogas en España. Delegación del Gobierno para el Plan Nacional sobre Drogas. Ministerio de Sanidad y Consumo, 2005, Madrid.
Observatorio Europeo de las Drogas y las Toxicomanías (OEDT). Informe anual 2005: El problema de la drogodependencia en Europa. 2005, Lisboa.
Organización Mundial de la Salud (OMS). Clasificación internacional de las enfermedades. 10.ª revisión. Organización Mundial de la Salud, 1992, Geneva.
Pacifici R, Zuccaro P, Pichini S, Roset PN, Poudevida S, Farré M, Segura J, De la Torre R. Modulation of the immune system in cannabis users. JAMA. 2003; 289:1929-31.
Patton GC, Coffey C, Carlin JB, Degenhardt L, Lynskey M, Hall W. Cannabis use and mental health in young people: cohort study. BMJ. 2002 Nov 23;325(7374):1195-8.
Pertwee R. receptors and pharmacodynamics: natural and synthetic cannabiniods and endocannabinoids. Guy G.W., Whitlle B.A, Robson P.J, editors. The medicinal uses of cannabis and cannabinoids. London: Pharmaceutical Press; 2004 p. 103-117.
Pistis M, Serra S, Pillolla G, Melis M, Muntoni AL, Gessa GL. Adolescent exposure to cannabinoids induces long-lasting changes in the response to drugs of abuse of rat midbrain dopamine neurons. Biol Psychiatry. 2004. Jul 15;56(2):86-94.
Poole R, Brabbins C. Drug induced psychosis. Br J Psychiatry 1996; 168: 135- 138.
Pope HG Jr, Gruber AJ, Turgelun-Todd D. The residual neuropsychological effects of cannabis: the current status of research. Drug and Alcohol Dependence. 1995;38:25-34.
Pope HG Jr, Gruber AJ, Hudson JI, Huestis MA, Yurgelun-Todd D. Neuropsychological performance in long-term cannabis users. Arch Gen Psychiatry. 2001;58:909-915.
Pope HG Jr, Gruber AJ, Hudson JI, Cohane G, Huestis MA, Yurgelun-Todd D. Early-onset cannabis use and cognitive deficits: what is the nature of the association. Drug Alcohol Depend 2003;69:303-310.
Ramaekers JG, Berghaus G, Van Laar M, Drummer OH. Dose related risk of motor vehicle crashes after cannabis use. Drug and Alcohol Dependence 2004; 73: 109-111.
Ramaekers JG, Robbe H, O’Hanlon J. Marijuana, alcohol and actual driving performance. Human Psychopharmacology: Clinical and Experimental 2000; 15: 551-558.
Raphael B, Wooding S, Stevens G, Connor J. Comorbidity: cannabis and complexity. J Psychiatric Practice 2005; 11:161-176.
Rogers RD, Robbins TW. Investigating the neurocognitive deficits associated with chronic drug misuse. Curr Opin Neurobiol. 2001;11:250-257.
Saso L. Effects of drug abuse on sexual response. Ann Ist Super Sanita 2002;38: 289-96.
Schifano F, Deluca P, Baldacchino A, Peltoniemi T, Scherbaum N, Torrens M et al. (on behalf of the Psychonaut 2002 research group).: Drugs on the web; the Psychonaut 2002 EU project. Prog Neuropsychopharmacol Biol Psychiatry. (accepted).
Schneider M, Koch M. Chronic pubertal, but not adult chronic cannabinoid treatment impairs sensorimotor gating, recognition memory, and the performance in a progressive ratio task in adult rats. Neuropsychopharmacol 2003; 28: 1760-1769.
Semple DM, McIntosh AM, Lawrie SM. Cannabis as a risk factor for psychosis: systematic review. J Psychoapharmacology 2005; 19: 187-194.
Sidney S. Cardiovascular consequences of marijuana use. J Clin Pharmacol. 2002;42(11 Suppl):64S-70S.
Smit F, Bolier L, Cujipers P. Cannabis use and the risk of later schizophrenia: a review. Addiction. 2004 Apr;99(4):425-30.
Solowij N, Stephens RS, Roffman RA, Babor T, Kadden R, Miller M, Christiansen K, McRee B, Vendetti J; Marijuana Treatment Project Research Group. Cognitive functioning of long-term heavy cannabis users seeking treatment. JAMA. 2002; 287:1123-1131.
Stefanis NC, Delespaul P, Henquet C, Bakoula C, Stefanis CN, Van Os J. Early adolescent cannabis exposure and positive and negative dimensions of psychosis. Addiction 2004;99(10):1333-1341.
Stephens RS, Roffman RA, Simpson EE: Treating adult marijuana dependence: a test of the relapse prevention model. J Consult Clin Psychology 1994, 62: 92-99.
Stephens RS, Roffman RA, Curtin L: Extended versus brief treatment for marijuana use. J Consult Clin Psychology 2000, 68:898-908.
Swift W, Hall W, Copeland J. One year follow-up of cannabis dependence among long-term users in Sydney, Australia. Drug Alcohol Depend 2000; 59: 309-318.
Thomas H. A community survey of adverse effects of cannabis use. Drug Alcohol Depend 1996; 42: 201-207.
Thomas H. Psychiatric symptoms in cannabis users. Br J Psychiatry 1993; 163: 141-149.
Troisi A, Pasini A, Saracco M et al. Psychiatric symptoms in male cannabis users not using other illicit drugs. Addiction 1998; 93: 487-492.
Tunving K. Psychiatric effects of cannabis use. Acta Psychiatr Scand 1985; 72: 209-217.
United Nations. Office on Drugs and Crime. 2004 World Drug Report. Viena United Nations 2005.
Van Os J, Bak M, Hanssen M, Bijl RV, de Graaf R, Verdoux H. Cannabis use and psychosis: a longitudinal populationbased study. Am J Epidemiol 2002; 156(4):319-327.
Veen ND, Selten JP, van der Tweel I, Feller WG, Hoek HW, Kahn RS. Cannabis use and age at onset of schizophrenia. Am J Psychiat 2004;161(3):501-506.
Verdejo-García A, López-Torrecillas F, Jiménez CO, Pérez-García M. Clinical implications and methodological challenges in the study of the neuropsychological correlates of cannabis, stimulant, and opioid abuse. Neuropsychol Rev. 2004;14:1-41.
Verdoux H, Gindre C, Sorbara F, Tournier M, Swendsen JD. Effects of cannabis and psychosis vulnerability in daily life: an experience sampling test study. Psychol Med 2003; 33(1):23-32.
Von Sydow K, Lieb R, Pfister H, Hofler M, Sonntag H, Wittchen HU. The natural course of cannabis use, abuse and dependence over four years: a longitudinal community study of adolescents and young adults. Drug Alcohol Depend 2001; 64: 347-361.
Wachtel SR, ElSohly MA, Ross SA, Ambre J, de Wit H. Comparison of the subjective effects of Delta(9)-tetrahydrocannabinol and marijuana in humans. Psychopharmacology (Berl). 2002;161:331-9.
Wax, PM: Just a Click Away: Recreational Drug Web Sites on the Internet. Pediatrics 2002;109:96.
Weiner MD, Sussman S, McCuller WJ, Lichtman K. Factors in marijuana cessation among high risk-youth. J Drug Education 1999; 29: 337-357.
Weiser M, Knobler HY, Noy S, Kaplan Z. Clinical characteristics of adolescents later hospitalized for schizophrenia. Am J Med Genet 2002;114(8):949-955.
Zammit S, Allebeck P, Andreasson S, Lundberg I, Lewis G. Self reported cannabis use as a risk factor for schizophrenia in Swedish conscripts of 1969: historical cohort study. Brit Med J 2002;325(7374):1199.
Sponsored Links : Metro Flyer, Real Canadian Superstore Flyer, Shoppers Drug Mart Flyer, Aldi Nord Prospekt, Lidl Prospekt